Suivez-nous sur les réseaux sociaux !
Sommaire du chapitre :
Publications
Chapitre 21 – Item 331 : Arrêt cardiocirculatoire
I. Définitions
II. Notions de chaîne de survie, défibrillation
III. Étiologies
IV. Diagnostic
V. Conduite à tenir en pratique
VI. Pronostic et survie à la phase préhospitalière
VII. Conditionnement hospitalier et pronostic à la phase hospitalière
Situations de départ
28 Coma et troubles de conscience (diagnostic différentiel).
38 État de mort apparente.
50 Malaise/perte de connaissance.
159 Bradycardie.
160 Détresse respiratoire aiguë.
161 Douleur thoracique.
165 Palpitations.
166 Tachycardie.
185 Réalisation et interprétation d’un électrocardiogramme (ECG).
Hiérarchisation des connaissances
| Rang | Rubrique | Intitulé | Descriptif |
|---|---|---|---|
| Définition | Définir un arrêt cardiocirculatoire | Connaître la définition OMS et l’identification (diagnostic positif = absence de réponse + ventilation inefficace) de l’arrêt cardiorespiratoire | |
| Définition | Définir la chaîne de survie | Connaître les différents maillons de la chaîne de survie | |
| Prévalence, épidémiologie | Connaître l’incidence et le pronostic de l’arrêt cardiocirculatoire chez l’adulte et l’enfant (non traité ici) | Incidence de reprise d’activité cardiaque spontanée, survie hospitalière, survie globale, pronostic fonctionnel | |
| Étiologies | Connaître les principales étiologies d’arrêt cardiocirculatoire chez l’adulte et chez l’enfant (non traité ici) | Connaître les principales étiologies, la prééminence de l’origine coronarienne | |
| Définition | Connaître le no-flow et low-flow | Connaître les notions du no-flow et low-flow | |
| Prise en charge | Connaître les besoins de ventilation de base | Connaître la technique d’oxygénation avec canule de Guédel ; savoir que la ventilation de l’adulte n’est pas prioritaire ; savoir que la ventilation de l’enfant/nourrisson est primordiale (non traitée ici) | |
| Prise en charge | Connaître l’algorithme universel de réanimation cardiopulmonaire de l’adulte | ||
| Prise en charge | Connaître les principes d’utilisation d’un scope/défibrillateur manuel/semi-automatique | Reconnaître les rythmes chocables, les dissociations électromécaniques, les asystolies Principes d’utilisation du défibrillateur manuel, et semi-automatique |
|
| Prise en charge | Connaître les voies d’abord vasculaires d’urgence | Voie veineuse périphérique, voie intra-intra-artérielle | |
| Prise en charge | Connaître le traitement médicamenteux (adrénaline) de la prise en charge initiale d’un rythme non chocable | Connaître les indications, la posologie et la séquence du vasopresseur de référence (adrénaline) et de l’antiarythmique de référence (amiodarone) | |
| Prise en charge | Connaître les traitements médicamenteux de la réanimation cardiopulmonaire | ||
| Prise en charge | Connaître les modalités diagnostiques et de traitement étiologique de l’arrêt cardiocirculatoire | Prise en charge des causes réversibles : connaître les étiologies et les principes de prise en charge, indications de la coronarographie | |
| Prise en charge | Connaître les critères d’arrêt de la réanimation | ||
| Prise en charge | Connaître l’algorithme universel de réanimation cardiopulmonaire de l’enfant* | ||
| Identifier une urgence | Arrêt cardiorespiratoire chez l’enfant : épidémiologie et mécanisme de l’ACR chez l’enfant* | ||
| Prise en charge | Principes de la prise en charge de l’arrêt cardiorespiratoire de l’enfant : premières minutes* | ||
![]() Les recommandations actuelles de prise en charge de l’arrêt cardiocirculatoire (ou arrêt cardiorespiratoire) en France reposent sur des recommandations déjà anciennes de la Société française d’anesthésie-réanimation (2009) et sur les recommandations européennes de 2015 du Comité européen de réanimation (ERC) regroupant les Sociétés européennes de cardiologie et de réanimation. La Société française de réanimation et la Société française de médecine d’urgence adoptent ces recommandations.
Les recommandations actuelles de prise en charge de l’arrêt cardiocirculatoire (ou arrêt cardiorespiratoire) en France reposent sur des recommandations déjà anciennes de la Société française d’anesthésie-réanimation (2009) et sur les recommandations européennes de 2015 du Comité européen de réanimation (ERC) regroupant les Sociétés européennes de cardiologie et de réanimation. La Société française de réanimation et la Société française de médecine d’urgence adoptent ces recommandations.
Ces recommandations européennes devraient être revues prochainement prenant en compte notamment les possibilités d’assistance extracorporelle déportées à distance des structures hospitalières. Des mises à jour sont néanmoins réalisées régulièrement. En 2019 a été publiée une mise à jour du comité de liaison international sur la réanimation (ILCOR) et des recommandations américaines ont été éditées en 2021.
Les arrêts cardiorespiratoires (ACR) extra-hospitaliers sont à l’origine de 300 000 décès par an aux États-Unis. En Europe, les décès sont évalués à 500 000 par an. En France, la fréquence des décès par ACR est de 40 000 par an, soit une incidence de 0,75 ‰ dans la population générale.
L’arrêt cardiorespiratoire, s’il est prolongé au-delà de quelques minutes, aboutit très rapidement au décès du patient. Au-delà de 5 minutes d’arrêt cardiaque, la survie est de l’ordre de 7 à 8 %. Au-delà de 10 minutes, elle est proche de 0 (cf. fig. 21.1).
Ce pourcentage de survie s’est peu amélioré dans les 40 dernières années. La survie sans séquelles notamment neurologiques est de l’ordre de 2 à 4 %
La survie des arrêts intra-hospitaliers est plus élevée, de 40–50 %, mais la mortalité reste importante.
Fig. 21.1. ![]() Probabilité de survie en fonction de la durée de la réanimation cardiopulmonaire.
Probabilité de survie en fonction de la durée de la réanimation cardiopulmonaire.
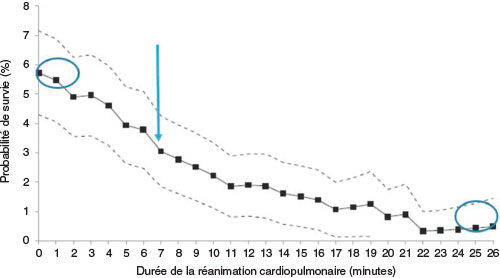
La probabilité de survie sans séquelle fonctionnelle, déjà très basse dès la survenue de l’arrêt cardiorespiratoire, décroît minute après minute et devient nulle après 30 minutes, d’où l’importance du témoin et de l’action immédiate de celui-ci, orienté si possible par un régulateur des urgences qui organise par téléphone la réanimation. Importance également de la formation aux premiers secours de la population générale dès le plus jeune âge avec un entretien régulier du niveau de compétences.
© Reynolds JC, Frisch A, Rittenberger JC, Callaway CW. Duration of resuscitation efforts and functional outcome after out-of-hospital cardiac arrest : when should we change to novel therapies ? Circulation. 2013 ; 128 (23) : 2488–94.
in Médecine cardiovasculaire, les Référentiels des Collèges, CNEC, SFC, 2022, 2e édition, Elsevier Masson
I Définitions
• La mort subite (OMS) est la mort instantanée, soudaine, subite qui correspond à une Maladie aiguë dont les symptômes qui la précèdent ne dépassent pas quelques minutes voire 1 heure au plus.
• L’arrêt cardiorespiratoire ou arrêt cardiocirculatoire (ACC) ou arrêt cardiaque (AC) correspond à la cessation de l’activité mécanique cardiaque, confirmée par l’absence de pouls et une apnée ou respiration agonique (gasping).
• L’arrêt cardiaque réfractaire est défini par l’absence de récupération d’une circulation spontanée après 30 minutes de réanimation médicale bien conduite. Cette définition française reste néanmoins discutée.
Le délai d’instauration des mesures de réanimation et de traitement (intervalle de temps entre la survenue de l’arrêt et le début de la réanimation) détermine le pronostic immédiat, intermédiaire et à distance de l’arrêt cardiaque. Ce délai est considéré par les experts comme étant le déterminant le plus important pour la survie.
![]() Ce délai est difficile, voire impossible à établir en l’absence de témoin. Cet intervalle de temps sans réanimation pendant lequel le patient est en état de « mort apparente » correspond à la période dite de no-flow (absence de mécanique cardiaque efficace).
Ce délai est difficile, voire impossible à établir en l’absence de témoin. Cet intervalle de temps sans réanimation pendant lequel le patient est en état de « mort apparente » correspond à la période dite de no-flow (absence de mécanique cardiaque efficace).
![]() Au-delà de 10 minutes d’arrêt sans hémodynamique (pouls et pression sanguine artérielle imprenables) et en dehors du cas particulier de l’hypothermie, le pourcentage de récupération et de survie des patients est très faible. Le diagnostic d’ACR doit donc être rapide et les premières mesures de réanimation instaurées immédiatement avant l’arrivée des premiers secours, souvent trop tardifs.
Au-delà de 10 minutes d’arrêt sans hémodynamique (pouls et pression sanguine artérielle imprenables) et en dehors du cas particulier de l’hypothermie, le pourcentage de récupération et de survie des patients est très faible. Le diagnostic d’ACR doit donc être rapide et les premières mesures de réanimation instaurées immédiatement avant l’arrivée des premiers secours, souvent trop tardifs.
![]() Le temps de réanimation sans rétablissement d’une hémodynamique convenable (pouls et pression artérielle stable) définit le temps de low-flow.
Le temps de réanimation sans rétablissement d’une hémodynamique convenable (pouls et pression artérielle stable) définit le temps de low-flow.
Les durées de no-flow et low-flow influencent de manière déterminante le pronostic. Tout doit être fait pour réduire ces temps :
• un temps de no-flow > 5 minutes est associé à un très mauvais pronostic (décès très élevé et séquelles fréquentes dans le cas de survie) ;
• au-delà de 10 minutes, la survie est quasi nulle et les récupérations hémodynamiques s’accompagnent généralement d’une évolution vers un état végétatif témoignant de l’altération irrémédiable des fonctions cérébrales supérieures. Au-delà de 10 minutes de no-flow, il est donc licite de s’interroger sur le caractère éthique d’une réanimation.
![]() Si la période de no-flow est brève, la durée du low-flow est moins déterminante au pronostic. À condition qu’elle soit débutée précocement et qu’elle soit bien réalisée et efficace, une réanimation longue peut s’accompagner d’une récupération fonctionnelle cardiaque et cérébrale.
Si la période de no-flow est brève, la durée du low-flow est moins déterminante au pronostic. À condition qu’elle soit débutée précocement et qu’elle soit bien réalisée et efficace, une réanimation longue peut s’accompagner d’une récupération fonctionnelle cardiaque et cérébrale.
Lorsque l’hémodynamique stable est récupérée (pouls et pression artérielle convenables), on parle d’ACR récupéré ou réanimé avec succès.
II Notions de chaîne de survie, défibrillation (cf. fig. 21.2 et fig. 21.3)
Fig. 21.2. ![]() Amélioration du pronostic en présence d’un rythme « chocable » (A) ou d’un témoin (B).
Amélioration du pronostic en présence d’un rythme « chocable » (A) ou d’un témoin (B).
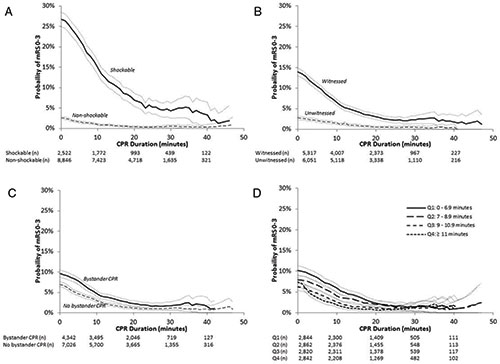
Le pronostic décroît néanmoins avec la durée de la réanimation pour devenir nul au-delà de 30 à 45 minutes, les chances de récupération sont meilleures en cas de témoin (C) et inversement proportionnelles à la durée de la réanimation (D).
© Reynolds JC, Grunau BE, Rittenberger JC, Sawyer KN, Kurz MC, Callaway CW. Association Between Duration of Resuscitation and Favorable Outcome After Out-of-Hospital Cardiac Arrest : Implications for Prolonging or Terminating Resuscitation. Circulation. 2016 ; 134 (25) : 2084–94.
in Médecine cardiovasculaire, les Référentiels des Collèges, CNEC, SFC, 2022, 2e édition, Elsevier Masson
Fig. 21.3. ![]() Les 6 maillons essentiels de la chaîne de survie : le témoin qui prévient les secours et débute la réanimation sous leur contrôle, le massage (dégagement des voies aériennes mais pas de bouche-à-bouche), la défibrillation dès que possible lorsque le rythme est « chocable », le transport vers une structure de réanimation adaptée, les mesures intrahospitalières de réanimation et le rétablissement.
Les 6 maillons essentiels de la chaîne de survie : le témoin qui prévient les secours et débute la réanimation sous leur contrôle, le massage (dégagement des voies aériennes mais pas de bouche-à-bouche), la défibrillation dès que possible lorsque le rythme est « chocable », le transport vers une structure de réanimation adaptée, les mesures intrahospitalières de réanimation et le rétablissement.

Finalement, le pronostic dépend de l’étiologie, du lieu de survenue intra ou extra-hospitalier, de la présence d’un témoin, de la rapidité des mesures immédiates de réanimation qui réduit la durée de no-flow et, à un moindre degré, de la durée de la réanimation.
© American Heart Association 2021.
in Médecine cardiovasculaire, les Référentiels des Collèges, CNEC, SFC, 2022, 2e édition, Elsevier Masson
A Principe de « chaîne de survie »
Le principe de chaîne de survie est essentiel. La rapidité de la mise en œuvre de cette chaîne et la complémentarité des différents maillons sont les gages de cette survie. Le concept de « chaîne de survie » a été décrit par Cummins en 1991 qui précise les 4 étapes de la réanimation d’un patient en ACR :
• les deux premiers maillons relèvent du grand public :
– l’alerte précoce dès le diagnostic fait par le témoin en composant le 15,
– la réanimation cardiopulmonaire (RCP) précoce,
• le troisième maillon, la défibrillation précoce, la plus précoce possible, peut être pratiquée en France non seulement par les médecins mais aussi par les infirmières, les secouristes et les ambulanciers depuis le décret 97–239 du 27 mars 1998. Depuis peu, il y a généralisation de défibrillateurs semi-automatiques dans les lieux publics notamment (gares, aéroports, stades, grandes administrations, etc.). On devrait pouvoir dans un bon nombre de cas obtenir le retour à un rythme efficace avant l’arrivée de l’équipe médicale. Il faut souligner malgré tout que le nombre de défibrillateurs « publics » reste bas en France, notamment dans les cabinets médicaux. Leur localisation est imprécise, mal connue et non systématisée. Néanmoins, un effort d’équipement important des lieux publics a été fait ces dernières années : stades, gares, aéroports, centres administratifs tels que les mairies. De nombreuses postes, pharmacies ou centres commerciaux sont équipés ;
• le quatrième élément de la chaîne est la RCP spécialisée commencée sur place par l’équipe du SMUR ;
• le cinquième maillon correspond à la prise en charge hospitalière réanimatoire de haut niveau, traitement de la cause de l’AC si possible, hypothermie contrôlée, assistance circulatoire, corrections des désordres métaboliques, etc. ;
• le 6e maillon concerne le rétablissement.
Une solide chaîne de survie peut améliorer considérablement les chances de survie et de rétablissement d’un patient victime d’un arrêt cardiocirculatoire
En France, les trois premiers maillons sont faibles puisque seulement 10 à 15 % de la population a reçu une formation ou une initiation à la RCP. Néanmoins, ce pourcentage s’accroît par la mise en place d’initiation dès le plus jeune âge.
Les études montrent l’importance de ces trois premiers maillons non seulement pour le pronostic vital mais aussi pour prévenir ou minimiser les séquelles neurologiques.
B Défibrillation, asystolie, massage
La fibrillation ventriculaire (FV) (cf. fig. 21.4 et fig. 21.5) représente le mode électrique initial d’arrêt cardiocirculatoire le plus fréquent et le choc électrique externe (CEE) son seul traitement efficace et potentiellement durable.
Fig. 21.4. ![]() Exemple d’électrocardiogramme de fibrillation ventriculaire.
Exemple d’électrocardiogramme de fibrillation ventriculaire.
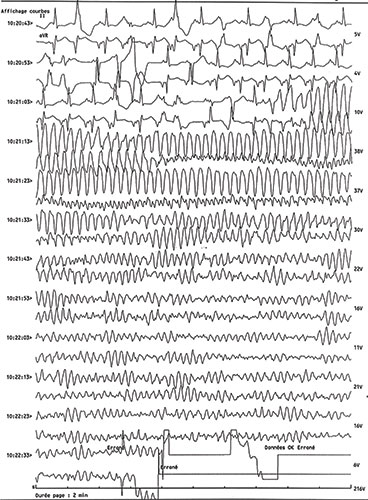
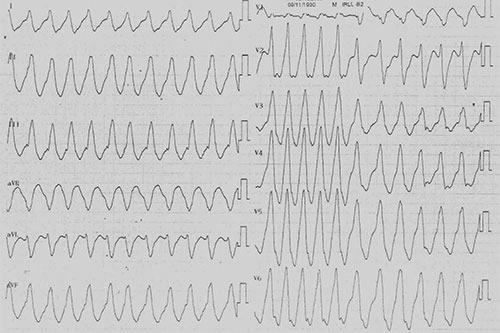
Fig. 21.5. ![]() Exemple d’électrocardiogramme de tachycardie ventriculaire.
Exemple d’électrocardiogramme de tachycardie ventriculaire.
La personne en arrêt cardiocirculatoire a pu présenter des prodromes à type de palpitations ou une douleur thoracique. Elle peut fréquemment avoir des antécédents connus de maladie coronarienne ou d’insuffisance cardiaque et peut prendre des médicaments qui ont pu faciliter l’arrêt cardiaque. Le pronostic dépend de la rapidité de la réalisation du CEE. La défibrillation consiste à faire passer à travers le cœur un courant électrique qui entraîne la dépolarisation simultanée d’une masse critique de cellules myocardiques interrompant les phénomènes de réentrée et donc la fibrillation ou la tachycardie ventriculaire.
Les défibrillateurs utilisant les ondes biphasiques (CEE délivré jusqu’à 200 J) remplacent aujourd’hui les défibrillateurs à ondes monophasiques (CEE délivré à 360 J). Ils sont reconnus comme plus sûrs et plus efficaces.
![]() Les défibrillateurs semi-automatiques (DSA) permettent d’administrer des CEE aux patients le nécessitant avant même l’arrivée des équipes médicales. Ils permettent de gagner un temps précieux. Le DSA analyse le rythme cardiaque du patient et porte l’indication de la défibrillation.
Les défibrillateurs semi-automatiques (DSA) permettent d’administrer des CEE aux patients le nécessitant avant même l’arrivée des équipes médicales. Ils permettent de gagner un temps précieux. Le DSA analyse le rythme cardiaque du patient et porte l’indication de la défibrillation.
Les taux de patients en FV survivant après une défibrillation sont respectivement de 25 % pour un délai de réalisation de la défibrillation de 7 à 10 minutes après l’arrêt cardiaque, de 35 % pour un délai de 4 à 6 minutes et de 40 à 60 % pour un délai de 1 à 3 minutes. Au-delà de 10 minutes de fibrillation ou d’arrêt, le taux de récupération d’un rythme cardiaque permettant une hémodynamique efficace est inférieur à 5 % et la survie sans séquelle neurologique lourde très rare.
![]() Idéalement, le premier choc électrique externe doit donc pouvoir être délivré dans les 3 minutes qui suivent l’arrêt si le diagnostic est rapide et l’accès au défibrillateur simple. À défaut et dans tous les cas, il faut débuter un massage cardiaque externe permettant de maintenir un degré minimal d’oxygénation tissulaire.
Idéalement, le premier choc électrique externe doit donc pouvoir être délivré dans les 3 minutes qui suivent l’arrêt si le diagnostic est rapide et l’accès au défibrillateur simple. À défaut et dans tous les cas, il faut débuter un massage cardiaque externe permettant de maintenir un degré minimal d’oxygénation tissulaire.
Le massage cardiaque permet transitoirement, en l’absence de défibrillateur ou d’efficacité de la défibrillation, de maintenir une mécanique cardiaque et une circulation vers les organes périphériques, en premier lieu le cerveau. Malheureusement, au moment du début de la RCP, la fibrillation ventriculaire n’est observée que dans 40 à 70 % des cas (selon la rapidité de mise en œuvre de la RCP). Lorsqu’elle est absente, le patient est en asystolie.
![]() L’asystolie (cf. fig. 21.6) témoigne soit d’une étiologie extra-cardiaque, soit le plus souvent d’une période de no-flow assez longue. La FV se dégrade (large maille puis petite maille sur le tracé) progressivement pour laisser place à un tracé électrique plat d’asystolie. L’asystolie initiale dès la survenue de l’arrêt cardiaque est assez rare mais possible. L’asystolie est un facteur pronostic péjoratif.
L’asystolie (cf. fig. 21.6) témoigne soit d’une étiologie extra-cardiaque, soit le plus souvent d’une période de no-flow assez longue. La FV se dégrade (large maille puis petite maille sur le tracé) progressivement pour laisser place à un tracé électrique plat d’asystolie. L’asystolie initiale dès la survenue de l’arrêt cardiaque est assez rare mais possible. L’asystolie est un facteur pronostic péjoratif.
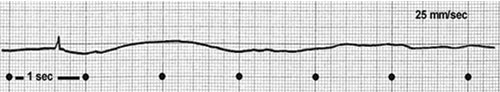
![]() Bien entendu, en cas d’asystolie constatée, la prise en charge repose sur le massage et non sur la défibrillation.
Bien entendu, en cas d’asystolie constatée, la prise en charge repose sur le massage et non sur la défibrillation.
![]() Le patient étant en arrêt cardiocirculatoire sans pouls ni pression artérielle, la reconnaissance entre asystolie et FV repose sur l’ECG ou un enregistrement continu sur un scope (généralement 1 à 3 dérivations). L’existence d’une activité électrique sans activité mécanique est appelée dissociation électromécanique. L’absence d’activité mécanique (pouls et pression sanguine artérielle restant imprenables) traduit un cœur généralement agonique sans contractilité efficace et doit conduire à poursuivre le massage même en présence d’une activité électrique.
Le patient étant en arrêt cardiocirculatoire sans pouls ni pression artérielle, la reconnaissance entre asystolie et FV repose sur l’ECG ou un enregistrement continu sur un scope (généralement 1 à 3 dérivations). L’existence d’une activité électrique sans activité mécanique est appelée dissociation électromécanique. L’absence d’activité mécanique (pouls et pression sanguine artérielle restant imprenables) traduit un cœur généralement agonique sans contractilité efficace et doit conduire à poursuivre le massage même en présence d’une activité électrique.
En l’absence d’ECG, les DSA utilisés pour défibriller analysent le rythme et ne délivrent le choc électrique que si le rythme est « chocable » (FV, flutter ventriculaire ou TV à fréquence élevée).
III Étiologies
![]() La cause immédiate la plus fréquente de survenue d’un arrêt cardiocirculatoire est une FV d’étiologie le plus souvent ischémique, conséquence soit de la constitution en cours d’une nécrose myocardique, soit d’un trouble du rythme ventriculaire induit par une séquelle ancienne d’infarctus.
La cause immédiate la plus fréquente de survenue d’un arrêt cardiocirculatoire est une FV d’étiologie le plus souvent ischémique, conséquence soit de la constitution en cours d’une nécrose myocardique, soit d’un trouble du rythme ventriculaire induit par une séquelle ancienne d’infarctus.
Le patient peut donc avoir présenté une FV d’emblée ou une TV qui s’est dégradée secondairement en FV en quelques minutes. Le trouble du rythme peut survenir au repos ou à l’effort.
Viennent ensuite les bradycardies extrêmes (bloc atrioventriculaire de haut grade, cf. fig. 21.7) et les asystolies (cf. fig. 21.6). En fonction du délai de prise en charge, les constatations initiales peuvent différer. Les causes cardiaques ou cardiovasculaires sont les plus fréquentes.
Fig. 21.7. ![]() Exemple d’électrocardiogramme de bradycardie extrême par bloc atrioventriculaire.
Exemple d’électrocardiogramme de bradycardie extrême par bloc atrioventriculaire.

A Syndromes coronariens aigus inauguraux
La pathologie coronarienne représente une grande part des étiologies des ACR. Elle en est la principale étiologie. L’arrêt cardiaque peut être précédé par une douleur thoracique qui témoigne de l’ischémie.
En effet, des lésions athéromateuses compliquées par une rupture de plaque et une thrombose coronarienne ont été fréquemment mises en évidence par des autopsies ou des coronarographies réalisées au décours de morts subites.
Le taux de lésions coronariennes dans les causes de mort subite varie entre 40 et 77 % selon les études.
B Autres étiologies cardiaques et vasculaires
![]() Ce sont :
Ce sont :
• les cardiomyopathies :
– cardiomyopathie hypertrophique particulièrement dans les formes familiales et/ou obstructives (la mort subite survient fréquemment au cours d’un effort, mais pas exclusivement),
– cardiomyopathie dilatée,
– dysplasie ventriculaire droite arythmogène,
– cardiopathies valvulaires (rétrécissement aortique essentiellement) ;
• les troubles du rythme ou de la conduction indépendants de toute anomalie cardiaque structurelle :
– FV idiopathique,
– syndrome de Brugada,
– troubles conductifs paroxystiques notamment du sujet âgé,
– syndromes du QT long congénitaux ou favorisés par les médicaments,
– syndromes du QT court congénitaux,
– troubles du rythme favorisés par l’existence d’une voie accessoire (syndrome de Wolff-Parkinson-White) ;
• une myocardite aiguë ;
• les cardiopathies congénitales et malformations vasculaires ;
• la tamponnade ;
• la dissection aortique ;
• l’embolie pulmonaire massive ;
• la rupture d’anévrisme, etc.
C Origines non cardiovasculaires
![]() D’après les études, ces étiologies représentent 5 à 25 % des cas. Les plus fréquentes sont les causes toxiques, traumatiques, les insuffisances respiratoires aiguës ou les noyades. Ces causes sont généralement de diagnostic plus aisé, orientées par le contexte.
D’après les études, ces étiologies représentent 5 à 25 % des cas. Les plus fréquentes sont les causes toxiques, traumatiques, les insuffisances respiratoires aiguës ou les noyades. Ces causes sont généralement de diagnostic plus aisé, orientées par le contexte.
IV Diagnostic
• Pour les témoins, le diagnostic repose sur la constatation d’un patient inconscient qui ne bouge plus, ne réagit plus et ne respire plus ou respire uniquement de manière très anormale (gasps).
• Pour le public formé au secourisme ou pour les premiers secours médicaux ou paramédicaux, il faut également constater l’absence de pouls carotidien ou fémoral.
Dès le diagnostic posé ou suspecté, il faut appeler le 15 et commencer les manœuvres de réanimation.
V Conduite à tenir en pratique
A Prise en charge pré-hospitalière avant l’arrivée de l’ambulance médicalisée
Les mesures de survie sont définies de façon universelle par l’acronyme ACD (cf. encadré 21.1). Dans l’attente des premiers soins médicalisés, les priorités de la réanimation sont les points A et C après avoir demandé de l’aide autour de soi et appelé le SAMU en composant le 15 :
• A : l’ouverture des voies aériennes supérieures se fait en basculant la tête en arrière et surélevant le menton, en vérifiant l’absence de corps étranger, que l’on retirera éventuellement avec les doigts en crochet ;
• C : le massage cardiaque externe (MCE) correctement réalisé est prioritaire pour limiter le temps de no-flow et améliorer le pronostic. La victime étant en décubitus dorsal, il consiste pour le sauveteur à appliquer le talon de sa main sur le centre du thorax de la victime et à réaliser des compressions de 4 à 5 cm d’amplitude à une fréquence de 100/min. Si plus d’un sauveteur est présent, il est conseillé de se relayer pour le MCE environ toutes les 2 minutes afin de limiter la fatigue et maintenir l’efficacité de la manœuvre ;
• D : si un matériel de défibrillation automatique externe (DSA) est disponible et si le sauveteur sait s’en servir, il doit être utilisé avant l’arrivée de l’ambulance médicalisée. Il est conseillé de poursuivre la réanimation encore 2 minutes après le choc, avant de vérifier la reprise d’une activité circulatoire efficace.
Encadré 21.1 ACD : mesures de prise en charge préhospitalière de l’arrêt cardiocirculatoire
| • A : Airway (maintien des voies aériennes libres) • C : Circulation (maintien d’une circulation) • D : Defibrillation (si le rythme initial est une tachycardie ou une fibrillation ventriculaire) |
Pour le A, les voies aériennes doivent être dégagées et rester libre. Dès que les secours arrivent ou en cas d’arrêt en milieu médicalisé, une canule de Guedel est mise en place dans la cavité buccale.
Les insufflations type bouche à bouche (B : Breathing) ne sont plus recommandées chez l’adulte contrairement à l’enfant et le nourrisson pour lesquels l’oxygénation reste essentielle.
Le MCE (massage cardiaque externe) reste prioritaire et son interruption doit être la plus limitée possible.
B Prise en charge par l’équipe médicalisée (généralement SMUR) : RCP médicalisée
1 Arrivée de l’équipe médicalisée
![]() Elle procède à :
Elle procède à :
• l’évaluation du pronostic de survie (cf. encadré 21.2) ;
• la réanimation médicalisée (cf. encadré 21.3) selon un alogrithme universel (voir figure jointe en annexe de ce chapitre).
La réanimation médicalisée permet :
• de réaliser une défibrillation si elle est appropriée.
• d’assurer une oxygénothérapie par ventilation invasive après intubation endotrachéale, qui doit être réalisée rapidement (ne pas interrompre le MCE plus de 30 secondes). En cas de difficulté d’intubation, il faut faire une ventilation au masque ;
• de poser une voie d’abord veineuse afin d’administrer des médicaments.
Encadré 21.2 Facteurs initiaux favorables à la réanimation au cours d’une mort subite
| • • Réanimation précoce • Rythme initial : fibrillation ventriculaire • Défibrillation rapide • Durée courte de la réanimation |
Encadré 21.3 Durant la réanimation médicalisée
| • • Minimiser les interruptions entre les compressions, y compris durant la période de mise en place de la ventilation • Oxygéner dès que possible • Utiliser un enregistreur de CO2 (capnographe) • Mettre en place des voies accès vasculaires (veineuse et si possible cathéter artériel pour évaluation permanente sanglante de la pression artérielle) • Administrer des médicaments (adrénaline, etc.) • Préparer le traitement étiologique s’il y a lieu (intoxication, revascularisation coronarienne) • Discuter mise en place d’une assistance circulatoire extracorporelle |
2 Médicaments utilisés
Vasoconstricteur : adrénaline
Historiquement, l’adrénaline a été le premier médicament utilisé au cours des arrêts cardiaques. Lors de la réanimation cardiorespiratoire, ses effets bénéfiques sont principalement dus aux récepteurs alpha-adrénergiques. La stimulation de ces récepteurs permet d’augmenter les débits sanguins myocardiques et cérébraux lors de la réanimation. L’importance des effets bêta-adrénergiques reste controversée car ils sont responsables d’une augmentation du travail myocardique et d’une réduction de la perfusion sous-endocardique. C’est un traitement médicamenteux incontournable dans les ACR réfractaires en asystolie.
Néanmoins, son impact dans l’amélioration du pronostic de survie et de réduction des séquelles neurologiques reste limité. Le pronostic est inversement corrélé à la quantité d’adrénaline utilisée durant la réanimation. Au-delà de 1 à 2 mg, la survie et faible et en cas de récupération d’une hémodynamique stable, la survie sans séquelles neurologiques lourdes est quasi inexistante.
La dose habituellement utilisée est de 1 mg toutes les 4 minutes par voie intraveineuse ou endotrachéale.
En cas de FV ou TV persistante sans efficacité circulatoire après le 1er choc électrique, l’adrénaline doit aussi être injectée après 2 minutes de réanimation immédiatement avant le 2e ou le 3e choc.
Antiarythmiques
Ils sont préconisés dans les ACR réfractaires avec troubles du rythme ventriculaire récidivants après des chocs électriques multiples (2 ou plus).
Amiodarone
L’amiodarone est une substance ayant une activité sur les canaux sodiques, potassiques et calciques, ainsi que des propriétés inhibitrices alpha et bêta-adrénergiques. Des études prospectives comparant le taux de récupération après l’administration d’amiodarone ou de lidocaïne ont conclu en faveur de l’amiodarone sur la survie à court terme.
L’amiodarone administrée par voie intraveineuse est recommandée pour les TV ou les FV réfractaires aux chocs électriques externes juste avant le 3e ou le 4e choc. La dose initiale est de 300 mg, diluée dans 20 à 30 mL de sérum salé isotonique et administrée rapidement. Des doses supplémentaires de 150 mg peuvent être renouvelées en cas de tachycardie ou de FV réfractaires ou récidivantes.
Lidocaïne
Elle a été utilisée pendant des années comme traitement des FV, de la TV réfractaire bien qu’elle n’ait jamais apporté de bénéfice à court ou long terme. Elle n’est utilisée que si l’on ne dispose pas d’amiodarone.
La posologie est de 1,5 mg/kg en injection intraveineuse lente. La dose totale ne doit pas être supérieure à 3 mg/kg.
Sulfate de magnésium
La posologie est de 2 g en IV directe en cas de torsades de pointes ou de suspicion d’hypomagnésémie.
Médicaments des bradycardies extrêmes
Atropine
La posologie recommandée lors de bradycardies sinusales extrêmes est de 1 mg répétée toutes les 3 à 5 minutes, jusqu’à une dose totale de 0,04 mg/kg.
Isoprénaline
Elle peut avoir un intérêt dans les bradycardies extrêmes, notamment les BAV du 3e degré sans hémodynamique efficace. La dose est de 5 ampoules à 0,2 mg diluées dans 250 cm3 de glucosé à 5 % dont le débit est à adapter à la fréquence pour un objectif classiquement supérieur ou égal à 50–60 battements/min.
L’atropine et l’isoprénaline ont un intérêt qui doit être restreint aux ACR dont l’étiologie est de façon certaine une étiologie conductive ou vagale maligne (bradycardies extrêmes avec des conséquences sur l’hémodynamique). Il s’agit d’ACR qui surviennent généralement en milieu intra-hospitalier ou médicalisé.
Agents métaboliques
L’arrêt cardiorespiratoire s’accompagne rapidement de désordres métaboliques témoignant de l’anoxie tissulaire et de la souffrance cellulaire. Il existe très rapidement (après 3 à 4 minutes d’ACR) une acidose métabolique et une hyperkaliémie qu’il faut compenser lors de la réanimation des ACR très prolongés.
L’administration de soluté de bicarbonate de sodium équimolaire 84 ‰ (dans le but d’obtenir une alcalinisation) reste discutée. L’ischémie lors d’un arrêt cardiorespiratoire induit une acidose métabolique. Celle-ci est le fait d’une diminution du débit sanguin. En rééquilibrant l’équilibre acido-basique, le bicarbonate de sodium aurait un effet positif sur la perfusion myocardique. Cependant, la plupart des études ne montrent pas d’amélioration significative.
L’alcalinisation est utilisée lors de situations particulières comme des réanimations prolongées, des hyperkaliémies, des acidoses préexistantes, des intoxications aux médicaments responsables d’élargissement marqué des QRS (phénobarbital et antidépresseurs tricycliques notamment).
Thrombolyse préhospitalière
On estime que 20 à 40 % des ACR compliquent un infarctus du myocarde (cause majeure des décès extra-hospitaliers des cardiopathies ischémiques aiguës).
D’autres études estiment que près de 70 % des patients réanimés pour un ACR préhospitalier présenteraient soit un IDM, soit une embolie pulmonaire massive.
![]() La thrombolyse préhospitalière n’est pas recommandée mais réservée au cas par cas, en cas d’infarctus du myocarde ou d’embolie pulmonaire massive avérés ou fortement suspectés.
La thrombolyse préhospitalière n’est pas recommandée mais réservée au cas par cas, en cas d’infarctus du myocarde ou d’embolie pulmonaire massive avérés ou fortement suspectés.
VI Pronostic et survie à la phase préhospitalière (cf. encadré 21.2)
Le pronostic est effroyable. La mort est quasi certaine si l’arrêt survient en l’absence d’un témoin. La plupart des études évaluent la survie globale des ACR à 5–20 % en différenciant les ACR survenant en milieu extra-hospitalier de ceux survenant en milieu intra-hospitalier dont le pronostic est meilleur.
Pour les ACR survenant en milieu extra-hospitalier, rétablir un rythme stable et efficace et une hémodynamique permettant au moins la perfusion cérébrale est un objectif majeur. Néanmoins, le succès de cet objectif n’assure pas en soi une survie prolongée et surtout un rétablissement ad integrum des fonctions cognitives.
| Seulement 20 % des patients arrivés « vivants » en milieu hospitalier peuvent ressortir sans séquelles neurologiques. |
L’ILCOR donne un taux moyen de patients sortant vivants de l’hôpital et pouvant reprendre une vie normale entre 2 et 10 % dans les grandes agglomérations ayant mis en place un réseau dense de DSA et une éducation de leur population (exemple néerlandais).
Le facteur essentiel pour la survie reste la prise en charge précoce de l’ACR. Les mécanismes de l’anoxie tissulaire entraînent une cascade de phénomènes à l’origine de nécrose cardiaque et cérébrale.
Le taux de survie décroît de 10 % pour chaque minute écoulée en l’absence de réanimation.
Un autre élément clé est la nature du trouble du rythme enregistré initialement.
L’ACR est le plus souvent la conséquence d’un trouble du rythme ventriculaire, FV d’emblée ou TV dégénérant secondairement en FV.
La FV est au départ à grosses mailles puis à petites mailles pour finir en tracé désorganisé, équivalent d’un tracé plat.
Le rapport ILCOR 2015 confirme que le rythme initial retrouvé par les réanimateurs est le plus fréquemment une FV (entre 70 et 80 % des cas) et, dans 15 à 20 % des cas, une bradycardie extrême incluant les blocs atrioventriculaires de haut degré et l’asystolie.
Pour mémoire, retenons que les FV conduisent, en l’absence de réanimation, au tracé plat d’asystolie.
Dans une étude menée sur 157 patients portant un enregistrement Holter ECG en ambulatoire et ayant présenté une mort subite (analyse du premier rythme) :
• 62 % ont présenté une FV ;
• 17 % ont présenté une bradycardie ;
• 13 % ont présenté une torsade de pointe ;
• 8 % ont présenté une TV.
Un autre essai a décrit le tracé de 205 patients ayant présenté un ACR, sans témoin, avec une réanimation par conséquent tardive :
• asystolie : 73 % ;
• dissociation électromécanique : 14 % ;
• FV : 13 %.
Les résultats apparemment divergents de ces études témoignent de l’importance du délai de diagnostic (immédiat versus retardé) sur le rythme observé lors de la réanimation. Ainsi, une asystolie est le marqueur d’un arrêt généralement déjà ancien. On estime que 50 % des FV se dégradent en asystolie entre la 4e et la 8e minute. L’asystolie est donc un marqueur de temps écoulé entre l’arrêt cardiaque et le diagnostic.
Le type de trouble du rythme est associé au pronostic, meilleur en cas de FV que d’asystolie.
VII Conditionnement hospitalier et pronostic à la phase hospitalière
| Après le retour à une circulation spontanée efficace, le pronostic des arrêts cardiaques dépend de la conservation ou de la récupération des fonctions myocardiques et surtout neurologiques. |
La phase intra-hospitalière a donc pour objectifs principaux la restauration partielle, au mieux complète des fonctions cardiaque et cérébrale.
On peut distinguer trois phases évolutives possibles intra-hospitalières pouvant influer sur le pronostic :
• Pendant les 12 premières heures : acidose, libération de radicaux libres et d’enzymes musculaires cardiaques lors de l’ischémie tissulaire ;
• de la 12e heure au 3e jour : répercussions de la souffrance sur les différents organes pouvant évoluer vers le syndrome de défaillance multiviscérale ;
• après le 3e jour : apparition d’un syndrome septique.
A Préservation de la fonction cardiaque
Dans un certain nombre de cas, la fonction cardiaque peut être transitoirement altérée (phénomène de sidération ou d’hibernation myocardique). Certains facteurs pré-hospitaliers sont reconnus comme favorisant la sidération myocardique :
• délai long avant la réanimation ;
• action des traitements vasopresseurs ;
• intensité et nombre de chocs électriques.
Le traitement de choix des troubles de la contractilité myocardique est la dobutamine, inotrope positif, mais elle n’a pu montrer aucune amélioration sur le pronostic.
Durant la phase intra-hospitalière, le monitoring par échocardiographie de la fonction cardiaque, parfois complété de la mesure des pressions invasives (cathéter de Swan-Ganz), est essentiel. La fonction myocardique peut être soutenue par des dispositifs de décharge ventriculaire gauche.
Sauf cas particulier, la contre pulsion intra-aortique à ballonnet n’est plus utilisée.
D’autres méthodes d’assistance circulatoire mécanique peuvent être utilisées, parfois même en phase pré-hospitalière : ECMO (assistance circulatoire par pompe extracorporelle), Impella® à débit suffisant : 3,5 ou 5 L/min (mise en place par voie percutanée ou chirurgicale d’une pompe intraventriculaire gauche).
Citons enfin, dans les facteurs indirects souvent utiles à la récupération myocardique, l’angioplastie d’éventuelles lésions coronariennes. La fréquence des étiologies coronariennes dans les ACR conduit à proposer dans les recommandations la réalisation d’une coronarographie et d’une angioplastie chez les patients pour lesquels ce diagnostic est avéré ou suspecté sur les données cliniques préalables : antécédents, douleur thoracique préalable à l’arrêt cardiaque rapportée par le témoin, ou sur l’aspect de l’ECG enregistré après la récupération d’une hémodynamique et d’un rythme qui soit compatible avec un syndrome coronarien aigu : sus-décalage ST, bloc de branche gauche, etc.
Bien entendu, coronarographie et éventuelle angioplastie sont réalisées en fonction du pronostic de survie évalué initialement notamment en fonction de la durée de no-flow.
Chez les patients de moins de 30 ans, la maladie coronarienne ayant une incidence faible, les causes cardiaques d’ACR sont principalement des troubles du rythme ventriculaire non ischémiques et des décompensations de cardiopathies congénitales.
B Préservation cérébrale et pronostic cérébral (cf. encadré 21.4)
Le cerveau souffre rapidement de l’anoxie cérébrale. Les lésions neurologiques apparaissent dès les premières minutes. Les neurones sont très sensibles aux variations de pression intracrânienne. Les mécanismes d’autorégulation peuvent disparaître lors d’un arrêt cardiorespiratoire. L’obtention d’une pression artérielle efficace conditionne le pronostic cérébral.
Encadré 21.4 Appréciation du pronostic cérébral
| Elle se fait sur l’évaluation régulière : • du score de Glasgow ; • de l’électroencéphalogramme ; • des potentiels évoqués sensitifs. Ces évaluations sont répétées ; leur spécificité et sensibilité s’affinent entre le 1er et le 3e jour. |
1 Oxygénation et ventilation
Elles sont en 1re ligne pour lutter contre l’hypoxie.
L’hypoxie et l’hypercapnie sont à l’origine d’une hypertension intracrânienne fatale. Cependant, le maintien d’une hyperoxie modérée permet de limiter la souffrance cérébrale.
2 Sédation
En mettant le tissu cérébral au repos, elle diminue les besoins en oxygène et permet de lutter contre l’œdème.
Il ne faut pas réveiller trop tôt après un ACR (24 à 48 heures de sédation).
3 Glycémie
Le glucose est l’élément nutritif unique du tissu cérébral. La glycorachie est maintenue constante dans le liquide cérébrospinal. Cependant, cette homéostasie est perturbée lors d’un ACR. L’hyperglycémie entraîne, par phénomènes osmotiques, un œdème cérébral. La lutte contre l’hyperglycémie est vitale.
4 Glucocorticoïdes
Les études n’ont pas mis au jour leur efficacité.
5 Régulation de la température (refroidissement ou cooling)
Le système nerveux central est sensible aux variations de température. Son métabolisme diminue de 8 % pour chaque °C en moins.
L’hyperthermie laisse des séquelles et doit donc être prévenue.
L’hypothermie modérée contrôlée autour de 34 °C préserve des lésions ischémiques. Elle est aujourd’hui systématiquement réalisée par des systèmes de refroidissement divers et maintenue au moins 24 heures.
Cette phase intra-hospitalière qui succède à l’arrêt cardiorespiratoire ressuscité ou réanimé avec succès constituerait le 5e maillon de la chaîne de survie : post-resuscitation care. La qualité de la prise en charge améliorerait très significativement le pronostic vital et fonctionnel, notamment cérébral.
In fine, au-delà du pronostic sombre initial des ACR, le pronostic des arrêts cardiaques récupérés est fréquemment marqué par les séquelles neurologiques qui vont de l’état végétatif aux séquelles motrices, cognitives, etc. lourdes qui nécessitent une longue rééducation et peuvent conduire à une perte plus ou moins totale d’autonomie, avec des conséquences sociales et familiales qu’il faut évaluer aux différentes étapes de la réanimation hospitalière.
Les échanges et l’information de la famille sont permanents mais contrôlés en limitant les interlocuteurs aussi bien du côté hospitalier que familial. La précocité de cette information, en éclairant les possibilités évolutives et les conséquences, permet d’éviter en général les situations conflictuelles. Dans les cas d’ACR récupéré avec mort cérébrale avérée, les possibilités de prélèvement d’organe nécessitent également l’information de la famille et l’absence d’inscription au registre national des refus.
La survenue malheureusement fréquente des ACR confronte le médecin au-delà de ses connaissances et de ses actions médicales, à la mise en pratique des grands principes de la déontologie médicale et de l’éthique. Cette responsabilité doit néanmoins être assumée dans un contexte d’équipe de soins.
Points-clés
| • • Il doit appeler le 15, puis et procéder aux mesures de survie ACD (A : libérer les voies aériennes, C : circulation (massage cardiaque externe), D : défibriller). • Les 3 principales étiologies d’ACR sont la fibrillation ventriculaire (FV), la tachycardie ventriculaire (TV) et l’asystolie. • La défibrillation est réalisée par choc électrique externe en cas de TV ou FV. • La 1re étiologie des arrêts cardiorespiratoires est représentée par les cardiopathies ischémiques aiguës ou anciennes sur séquelle d’infarctus. • L’adrénaline IV est utilisée en cas d’asystolie. • Les fonctions cérébrales doivent être préservées à la phase intra-hospitalière. • L’hypothermie modérée contrôlée autour de 34 °C préserve des lésions ischémiques cérébrales. • Le pronostic des ACR est catastrophique et le principal facteur pronostique est la durée de no-flow. • La récupération initiale d’une hémodynamique par le patient n’est pas synonyme de survie. • La survie est rare avec fréquemment des séquelles neurologiques. • L’information régulière des proches, de la famille sur le pronostic et l’évolution est essentielle. • La décision d’arrêt de réanimation est collégiale et orientée par les EEG répétés qui témoignent de la mort cérébrale. • L’arrêt de réanimation et le décès doivent bénéficier d’une préparation à l’annonce. • Un prélèvement d’organe si réanimation rapide et préservation de l’hémodynamique |
Notions indispensables et inacceptables
Notions indispensables
• La cause la plus fréquente des ACR est représentée par la FV survenant au cours des cardiopathies ischémiques (SCA récent ou séquelles d’infarctus).
• Le pronostic et les chances de survie sans séquelle sont faibles au-delà de 5 minutes de no-flow.
• Les DSA permettent de délivrer un CEE en cas d’ACR « chocable » (TV ou FV).
Notions inacceptables
• Ne pas connaître les mesures de survie définies de façon universelle par l’acronyme ACD (libération des voies aériennes, massage cardiaque, défibrillation).
Réflexes transversalité
• Item 14 – La mort.
• Item 201 – Transplantation d’organes : aspects épidémiologiques et immunologiques ; principes de traitement ; complications et pronostic ; aspects éthiques et légaux. Prélèvements d’organes et législation.
• Item 230 – Douleur thoracique aiguë.
• Item 231 – Électrocardiogramme : indications et interprétations.
• Item 236 – Troubles de la conduction intracardiaque.
• Item 237 – Palpitations.
• Item 332 – État de choc. Principales étiologies : hypovolémique, septique, cardiogénique, anaphylactique
• Item 339 – Syndromes coronariens aigus.
Partagez cette publication
Written by : SFC
Plus de publications de la SFC

INTELLIGENCE ARTIFICIELLE New Threshold for Defining Mild Aortic Stenosis Derived From Velocity-Encoded MRI in [...]

CARDIOLOGIE PÉDIATRIQUE The Cardiovascular Care of the Pediatric Athlete | Lire l'article JACC CARDIO-ONCOLOGIE [...]



